Эпигенетика. Как современная биология переписывает наши представления о генетике, заболеваниях и наследственности - Несса Кэри Страница 60
Эпигенетика. Как современная биология переписывает наши представления о генетике, заболеваниях и наследственности - Несса Кэри читать онлайн бесплатно
Экспрессия белка Blimp1 контролируется сложным взаимодействием активности Lin28 и let-7 [151]. Белок Blimp1 также регулирует, метилирующий гистоны фермент и класс белков PIWI. Белки PIWI, в свою очередь, связаны с другим типом коротких нкРНК, которые называются РНК PIWI [152]. нкРНК и белки PIWI, по-видимому, не играют большой роли в соматических клетках, но они требуются для продукции мужской эмбриональной линии клеток [153]. P1WI это аббревиатура словосочетания «Р element induced w/mpy testis» («индуцированная по родительской линии ослабленная мужская половая железа»). Если нкРНК PIWI и белки PIWI не взаимодействуют должным образом, половые железы у плода мужского пола не могут сформироваться.
Мы продолжаем встречать все больше и больше случаев пересечений и взаимодействий между нкРНК и эпигенетическими явлениями. Вспомните, что «генетические контрабандисты», ретротранспозоны, обычно метилируются в эмбриональной линии, что препятствует их активации. И PIWI принимают активное участие в определении мишеней этого метилирования ДНК [154] [155]. Значительное количество эпигенетических белков способны взаимодействовать с РНК. Связывание некодирующих РНК с геномом может являться общим механизмом, позволяющим направлять эпигенетические модификации на нужную хроматиновую область в определенном типе клеток [156].
Недавно нкРНК нашли свое место в теории Ламарка, в основе которой лежит концепция передачи унаследованных характеристик. В одном из экспериментов в оплодотворенные мышиные яйцеклетки были введены миРНК, мишенью которых был ключевой ген, отвечающий за рост ткани сердца. У мышей, развившихся из этих яйцеклеток, оказались увеличенные сердечные мышцы (кардиальная гипертрофия) вследствие того, что введение миРНК на ранних стадиях развития нарушило его нормальные процессы. Примечательно, что потомство этих мышей также продемонстрировало высокий процент кардиальной гипертрофии. Вероятно, это было вызвано тем, что аномальная экспрессия миРНК была восстановлена в процессе вырабатывания сперматозоидов у этих мышей. Изменений кода ДНК у них не наблюдалось, так что это был явный случай эпигенетического наследования при помощи миРНК [157].
Закон Мэрфи (если беде быть, то ее не миновать)
Но раз нкРНК настолько важны для функционирования клеток, мы, несомненно, сможем обнаружить целый ряд заболеваний, связанных с нарушением их деятельности. Разве не должны окружать нас многочисленные примеры того, что отклонения в производстве и экспрессии нкРНК ведут к клиническим расстройствам, отличным от болезней, связанных с импринтингом или репрессией хромосомы X? И да, и нет. Так как эти нкРНК являются в первую очередь регуляторными молекулами, действующими в сети, насыщенной компенсаторными механизмами, то их дефекты могут проявляться лишь в относительно легкой степени. Проблема, вытекающая из этого для исследователей, состоит в том, что большинство генетических экспериментов эффективны для идентификации явных фенотипов, вызываемых мутациями белков, но они оказываются менее пригодными для выявления менее очевидных отклонений.
Есть такая короткая нкРНК под названием ВС1, которая экспрессируется у мышей в определенных нейронах. Когда исследователи из университета Мюнстера в Германии удалили у мышей эту нкРНК, те продолжали выглядеть вполне здоровыми. Затем ученые перевели животных-мутантов из строго контролируемых лабораторных условий в более естественную для них среду. И тогда обнаружилось, что мутанты сильно отличаются от своих обычных родственников. Животные с большой неохотой исследовали территорию и демонстрировали сильное беспокойство [158]. Если бы ученые просто оставили их в клетках, то мы бы никогда и не узнали, что утрата нкРНК ВС1 в действительности оказывает огромное влияние на поведение. Это еще одно подтверждение уже известной нам истины: то, что мы видим, зависит от того, как мы на это смотрим.
Связь нкРНК с клиническими состояниями постепенно становится все более очевидной, подтверждением чему являются, по крайней мере, некоторые примеры. Есть такая порода овец, которая называется тексель, и наиболее ласковой характеристикой ее представительниц будет определение «коренастые». Овцы породы тексель славятся обилием мышечной массы, что делает честь животным, предназначенным для того, чтобы стать пищей. Своей мускулистостью эта порода обязана, по меньшей мере отчасти, изменению места присоединения миРНК к 3’ НТР определенного гена. Белок, кодируемый этим геном, называется миостатин, и обычно он замедляет рост мышечной ткани [159]. Результат, полученный при изменении единственного основания, показан на рисунке 10.4. Для наглядности размер овцы тексель намеренно преувеличен.
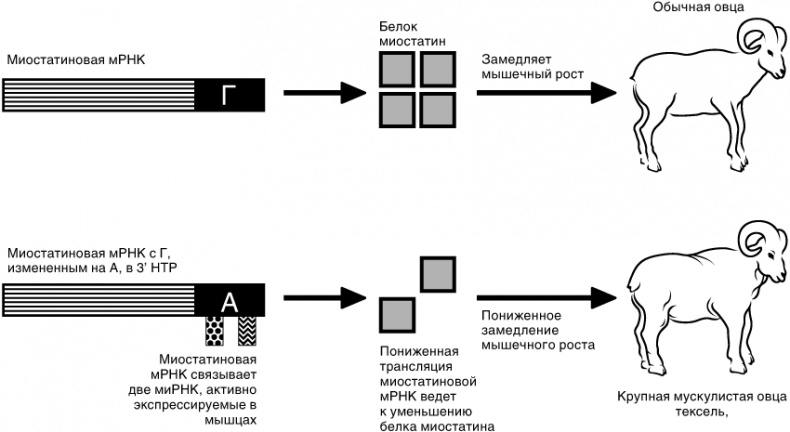
Рис. 10.4. Точечная мутация участка гена миостатина, не кодирующего белок, тем не менее оказывает мощное влияние на фенотип овцы породы тексель. Замена основания Г на А в миостатиновой мРНК приводит к связыванию двух определенных микроРНК. Это меняет экспрессию миостатина, в результате чего у овцы начинается бурный рост мышечном массы
Синдром Туретта является расстройством центральной нервной системы, при котором тикообразные подергивания мышц лица, шеи и плеч и непроизвольные движения губ и языка сочетаются с частым покашливанием и оплевыванием. При исследовании двух независимых пациентов, страдающих этим нарушением, обнаружилось одинаковое изменение единственного основания в 3’ НТР гена под названием SLITRKP [160]. Ген SLITRK1 необходим, следовательно, для нормального неврологического развития. Изменение основания у больных синдромом Туретта происходило на участке связывания с короткой нкРНК, которая называется miR-189. Это позволяет нам предполагать, что в критические моменты развития экспрессия SLITRK1 могла быть аномально понижена на этом участке связывания. Подобное изменение наблюдается всего лишь в нескольких случаях синдрома Туретта, но оно заставляет сделать вывод, что и у других пациентов, вероятно, происходило нарушение регуляции участков связывания миРНК на иных нейронных генах.
Жалоба
Напишите нам, и мы в срочном порядке примем меры.





Комментарии