ДНК. История генетической революции - Джеймс Д. Уотсон Страница 29
ДНК. История генетической революции - Джеймс Д. Уотсон читать онлайн бесплатно
Ознакомительный фрагмент
Сначала при помощи рестриктаз разрезали две неизмененные плазмиды. Затем эти плазмиды смешивались в одной пробирке, куда добавлялся фермент лигаза, которая должна была запустить склеивание обрезанных концевых остатков. Некоторые молекулы в пробирке под действием лигазы просто восстанавливали целостность – то есть склеивались два концевых остатка одной и той же плазмиды. Но иногда лигаза срабатывала так, что в разрезанную плазмиду попадали фрагменты ДНК другой плазмиды – так и получался желаемый гибрид. Когда эта задача была решена, требовалось внедрить все плазмиды в бактерии, и это успешно было проделано с использованием технологий Коэна. Полученные от рекомбинантов колонии выращивались на агаровых пластинах, покрытых одновременно тетрациклином и канамицином. Те плазмиды, которые просто восстановились свою структуру, по-прежнему обеспечивали устойчивость лишь к одному из двух антибиотиков, и, соответственно, бактерии с такими плазмидами не выживали в среде, содержащей два антибиотика. В такой среде могли выжить только бактерии с рекомбинантными плазмидами, сконструированными из двух имевшихся разновидностей ДНК, одна из которых кодировала устойчивость к тетрациклину, а другая – к канамицину.

Герб Бойер и Стенли Коэн – первые в мире генные инженеры
Следующий вызов сложившемуся в обществе укладу заключался в создании гибридной плазмиды с использованием ДНК не бактерий, а иного организма, например человека. В одном из первых успешных экспериментов ген африканских шпорцевых лягушек удалось добавить в плазмиду E. coli и трансплантировать ее в бактерию. Всякий раз при делении клеток в такой бактериальной колонии реплицировался лягушачий фрагмент ДНК. Если не применять сложную молекулярно-биологическую терминологию, а просто описать происходящее, то это выглядит как «клонирование ДНК лягушки» [5]. Как стало известно, ДНК млекопитающих также успешно клонируется. Ретроспективный анализ показал, что в этом нет ничего особенно удивительного: любой фрагмент ДНК – это, в конечном счете, просто ДНК, его химические свойства не изменяются в зависимости от источника. Вскоре стало понятно, что протоколы Коэна и Бойера, описывающие клонирование фрагментов ДНК, применимы к ДНК любого организма.
Таким образом, разворачивался уже второй этап молекулярно-биологической революции. На первом этапе мы стремились описать статус и функционал ДНК в клетке, затем, после получения рекомбинантной ДНК [6], появились реальные инструменты для вмешательства в работу ДНК и манипулирования ею. Был создан плацдарм для стремительного прогресса, а мы примерили на себя роли Творца. Полученные результаты пьянили: открывался огромный потенциал, позволявший глубоко погрузиться в тайны жизни и добиться успеха в борьбе с такими болезнями, как рак. Несмотря на то что работы Коэна и Бойера предоставили нам фантастические научные перспективы, – не открылся ли при этом ящик Пандоры? Не скрывалось ли в молекулярном клонировании какое-то неизвестное зло? Можно ли и далее беззаботно вшивать кусочки человеческой ДНК в E. coli, учитывая, какие огромные колонии этих бактерии обитают в «микробных джунглях» нашего кишечника? Что будет, если в кишечник проникнет видоизмененная бактерия? Короче говоря, можно ли, будучи в здравом уме, заткнуть уши и не слушать скептиков, заявляющих, что на глазах у всего научного мира мы творим бактерий-франкенштейнов?
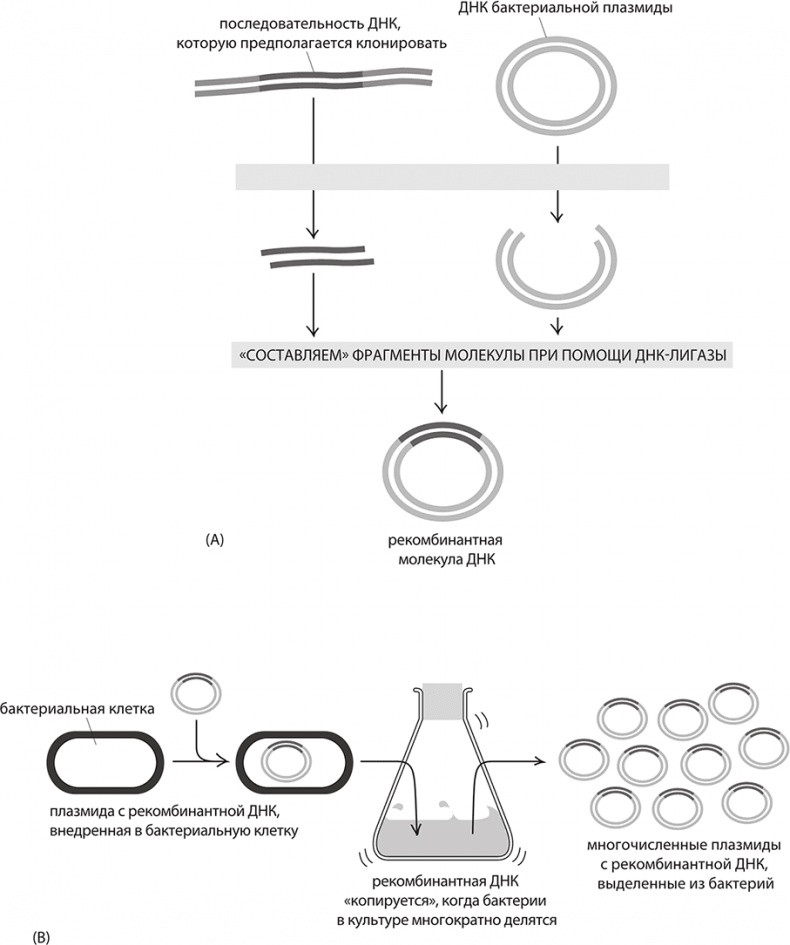
Рекомбинантная ДНК: суть клонирования гена. A. Бактериальные плазмиды оказались идеальным носителем для клонирования ДНК; разрезая одной и той же рестриктазой интересующую нас ДНК и плазмиду, можно вставлять интересующую нас ДНК в плазмиду, как деталь в пазл. B. Внедрив эту рекомбинантную плазмиду в бактерию, можно реплицировать в бактериальной культуре интересующий нас ген – на основе таких приемов развились генная инженерия, секвенирование ДНК и биотехнологическая индустрия

Кишечная палочка E. coli. Представляете, около 10 миллионов этих существ обитает в каждом грамме человеческого кала
В 1961 году удалось выделить обезьяний вирус SV40 (SV означает «обезьяний вирус») из почек макак вида резус, использовавшихся при разработке вакцины против полиомиелита. Хотя и считалось, что этот вирус никак не влияет на мартышек, в организме которых встречается, вскоре дальнейшие эксперименты показали, что вирус может вызывать рак у грызунов, а в определенных лабораторных условиях – даже в человеческих клетках. Поскольку кампания по вакцинации от полиомиелита проводилась с 1955 года и миллионы американских детей уже были заражены этим вирусом, новость действительно была тревожной. Что если, искореняя полиомиелит, мы случайно обрекли целое поколение на риск развития онкологических заболеваний? По-видимому, этого все-таки не случилось: эпидемия рака не разразилась, а SV40 в организме человека, судя по всему, не более патологичен, чем у мартышек. Тем не менее даже тогда, когда SV40 прочно обосновался в молекулярно-биологических лабораториях, оставались сомнения в его безопасности. Меня это особенно волновало, поскольку я к тому времени руководил лабораторией Колд-Спринг-Харбор, где появлялись все новые молодые ученые, работавшие с SV40 и зондировавшие с его помощью генетические основы рака.

Пол Берг и его вирусная «хонда»
Тем временем Пол Берг из Медицинской школы Стэнфордского университета усматривал в вирусе SV40 скорее возможности, чем опасности: он предвидел, что этот вирус удастся использовать для внедрения фрагментов ДНК в клетки млекопитающих. Вирус мог бы работать у млекопитающих как молекулярная система доставки лекарств, именно так, как действовали плазмиды у бактерий в опытах Стенли – Коэна. Однако если Коэн, в сущности, использовал бактерии как копировальные аппараты, позволяющие «увеличить» нужный фрагмент ДНК, то Берг рассматривал SV40 как средство для внедрения корректировочных генов людям, страдающим от генетических заболеваний. Берг опередил свое время. Он стал вдохновителем практики, которая сегодня именуется «генотерапия» и заключается во введении нового генетического материала в организм живого человека с целью сгладить унаследованные генетические расстройства.
Жалоба
Напишите нам, и мы в срочном порядке примем меры.





Комментарии