Нильс Бор. Квантовая модель атома - Хайме Наварро Страница 21
Нильс Бор. Квантовая модель атома - Хайме Наварро читать онлайн бесплатно
На макроскопическом уровне этого не происходит. Представим себе, как мы наблюдаем за тем, что находится внутри абсолютно темной комнаты. Мы можем взять фонарик, и если мы будем осторожными, наше наблюдение не окажет воздействия на содержимое комнаты. Но если мы захотим измерить содержимое атома, для его «освещения» будет использован поток света, энергия которого — того же порядка, что и у электронов внутри, поэтому мы получим информацию о результате взаимодействия света с электронами, а не о том, какими были электроны до облучения. Выходит, что на внутриатомном уровне измерение — это процесс, который изменяет саму систему и, следовательно, предоставляет информацию не о том, какой была эта система до наблюдения, а о том, какой она стала после.
Итак, принцип неопределенности — это отход от самого понятия траектории и местоположения. Другими словами, Гейзенберг, Бор и Паули считали, что физика должна сосредоточиться на начальных и конечных условиях изучаемых событий, а не на процессе, который они преодолевают, поскольку вмешаться в сам процесс означает изменить его. Это то же самое, что исследовать поведение воды в состоянии покоя в бассейне, погрузившись в нее. Изучаемое состояние будет полностью изменено, и любые полученные данные будут соответствовать не стоячей воде, а совокупности вода-пловец.
ЧАСТИЦЫ И ВОЛНЫ
Наряду с головоломкой о внутренней структуре атома физика начала XX века столкнулась с другой загадкой — с природой таких излучений, как свет, рентгеновские лучи и радиоактивность. Что такое свет? Что это за «объект*'? Вопрос завораживал натурфилософов эпохи Возрождения и Барокко, включая Галилея, Декарта и Ньютона, но они не пришли к окончательному соглашению. Из-за авторитета Ньютона в XVIII веке многие точно следовали его идеям и считали очевидным, что свет состоит из потока световых частиц. Хотя также были свидетельства, позволявшие предположить, что свет ведет себя как волна. В XIX веке тенденция изменилась, и особенно после работ Максвелла, подтвержденных в 1888 году Генрихом Герцем (1857-1894), уже никто не сомневался, что свет — это волна и что Ньютон ошибался.
Однако этот консенсус длился недолго. Рентгеновские лучи и у-излучение имели некоторые общие свойства с электромагнитным светом, но в других аспектах вели себя как частицы. Также в одной из своих статей 1905 года Эйнштейн предположил, что свет подчиняется постулату Планка и, следовательно, должен пониматься как совокупность «квантов света», частиц, которые позже назвали «фотонами». Ученые вновь оказались на распутье.
Известны два знаменитых комментария, демонстрирующих замешательство в среде физиков накануне Первой мировой войны и в первые послевоенные годы. Так, на лекции 1921 года Уильям Генри Брэгг (1862-1942) сокрушался, что физики находятся в полнейшей темноте:
«Должно быть, есть какой-то факт, абсолютно неизвестный нам, который, когда он будет открыт, произведет революцию в нашем представлении о связи между волнами, эфиром и материей. На данный момент мы вынуждены оперировать обеими теориями. По понедельникам, средам и пятницам мы пользуемся волновой теорией, а по вторникам, четвергам и субботам интерпретируем свет как потоки частиц».
Джозеф Джон Томсон, в свою очередь, пошутил, что волновая и корпускулярная теории похожи на «битву между тигром и акулой. Каждый из этих зверей самый сильный в своих владениях, но бесполезен на территории другого».
Конфликт двух теорий был разрешен в результате его расширения. В 1924 году молодой французский аристократ Луи де Бройль (1892-1987) защитил докторскую диссертацию, в которой применил теорию относительности к движению электронов. Движению последних, а следовательно и каждой частице, назначалась волна, то есть был сделан вывод, что иногда они ведут себя как волна. Сам Эйнштейн пришел в восторг от этой диссертации.
Следуя концепции Луи де Бройля, молодой преподаватель Цюрихского университета Эрвин Шрёдингер (1887-1961) развил настоящую механическую теорию электронов с помощью математики, характерной для изучения волн. Так Шрёдингер смог предсказать возможные квантовые состояния электронов в атоме. Гейзенберг сделал то же самое, но различие заключалось в способе. Если назначить каждому электрону волновую функцию, то волны могут взаимодействовать — как, например, две морские волны. Самое удивительное было в том, как Шрёдингер вводил квантовые числа в каждую волну, то есть в поведение электронов, поскольку он делал это на основе узлов гармонического колебания волн.
Представим себе струну, закрепленную с двух сторон. Она может колебаться различными стабильными способами, называемыми гармониками, как показано на рисунке 1. Самая простая основная гармоника — имеющая в качестве единственных неподвижных точек концы струны. Вторая гармоника — та, в которой есть еще одна неподвижная неколеблющаяся точка в середине струны. В третьей гармонике их две, и так далее.
Гениальность Шрёдингера состояла в том, что он связал узлы колебания со спектральными линиями атома водорода. Другими словами, узлы гармонических колебаний волновой функции, назначенной электрону, определялись как квантовые числа, которые Бор и Зоммерфельд ввели в свою модель атома. В формулировке Шрёдингера поведение электронов задано узлами назначенной им волновой функции; квантовые числа оказывались естественным образом связанными с этими узлами.
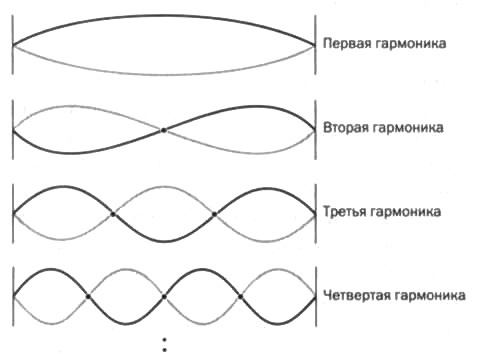
РИС. 1
ПРИНЦИП ДОПОЛНИТЕЛЬНОСТИ
С 1925 по 1926 год успех Института теоретической физики в Копенгагене был таким, что Бору пришлось расширить помещение. Здание, полное каменщиков, рабочих и небольшой армии ученых, — неплохая метафора происходящего в то время, ведь тогда изменялся сам фундамент физики. Однако, как это часто происходит с любым архитектурным проектом, планы не всегда совпадали. Точно так же не совпадали проекты, разработанные Гейзенбергом, Паули, Борном и Бором, с проектами Шрёдингера и де Бройля. Нужно было либо отказаться от одного из них, либо интерпретировать их так, чтобы совместить.
Бор убедил своего излюбленного собеседника Гейзенберга принять предложение преподавать в Копенгагене в течение года, чтобы иметь возможность продолжать закладку фундамента квантовой механики. Именно это и происходило в течение 1926-1927 учебного года. Частично реконструкция Института теоретической физики состояла в полной переделке жилой части здания, чтобы разместить гостивших ученых. Семья Боров, в свою очередь, перебралась в особняк по соседству. Гейзенбергу было поручено подготовить жилье к принятию приглашенных ученых, и тот смог оценивать преимущества работы рядом с Бором денно и нощно. Позже Гейзенберг вспоминал:
«Иногда Бор заходил в мою комнату в 8 или в 9 утра и спрашивал: «Что ты думаешь об этом?», затем он сразу же продолжал говорить и говорить, отвечая на вопрос, который сам же задал. И так до полуночи».
Одним из основных вопросов, которые беспокоили обоих физиков, было, конечно же, наличие двух теорий. Полностью различные по принципам, они были одинаково полезными. Это стало ясно, когда вскоре по прибытии в Копенгаген Гейзенберг решил проблему спектра гелия, применив методы Шрёдингера, а также принцип запрета и понятие спина. Настало время пригласить Шрёдингера, с которым Бор еще не был знаком лично, провести несколько дней в Копенгагене.
Жалоба
Напишите нам, и мы в срочном порядке примем меры.




Комментарии