Неопределенный электрический объект. Ампер. Классическая электродинамика. - Эугенио Мануэль Фернандес Агиляр Страница 17
Неопределенный электрический объект. Ампер. Классическая электродинамика. - Эугенио Мануэль Фернандес Агиляр читать онлайн бесплатно
КЛАССИФИКАЦИЯ ЭЛЕМЕНТОВ
Из-за отсутствия интереса научного сообщества к его работам Ампер на несколько месяцев отошел от химии. Однако новый статус академика заставил его вернуться к этой науке, и в 1815 году он посвятил значительное время исследованию, которое представил в следующем году в «Анналах химии и физики» в нескольких частях под названием «Эссе о естественной классификации простых тел». Так еще раз проявилась его страсть к классификации. Ампер пытался применить критерии ботаники, известные ему с юности, к химии и таким образом выстроить естественную классификацию простых тел, или элементов. Для этого он использовал таблицу из 33 элементов, составленную Лавуазье в 1789 году.
В 1815 году Ампер составил список из 48 элементов, которые разделил на 15 видов (сопоставимых с группами современной периодической таблицы) в соответствии с их свойствами. Он разделил вещества по трем родам: газолиты, лейколиты и хроиколиты. Хотя ученый не делил вещества на металлы и неметаллы, он указал, что газолиты являются неметаллами, тогда как лейколиты и хроиколиты — металлы. Газолиты включают в себя пять видов, и их главное свойство заключается в том, что они являются газообразными веществами или веществами, способными образовывать газы. Лейколиты также разделены на пять видов, это элементы с низкой температурой плавления. Наконец, хроиколиты имеют высокую температуру плавления, они тоже разделены на пять видов. Ампер использует суффикс -ид, который в греческом языке означает «схожий с»; так, название «бориды» означает «схожие с бором».

В Париже Ампер продемонстрировал большой интерес к химии, вызванный исследованиями Гемфри Дэви.

В 1824 году Ампер был назначен профессором физики в Коллеж де Франс.

Портрет Авогадро, который в 1811 году предложил понятие молекулы. В 1814 году такую же гипотезу выдвинул Ампер.

В 1789 году Лавуазье опубликовал «Элементарный курс химии», который сыграл важную роль в созданной Ампером классификации 48 элементов, которую он осуществил в 1815 году.
В классификации элементов Ампера (см. таблицу на странице 84) есть много плюсов и минусов. Ему удалось точно классифицировать известные в то время галоидные соли, которые находятся в колонке 17 периодической классификации: фтор (F), хлор (Сl) и йод (I). Он также правильно объединил известные в то время элементы, образующие щелочи, то есть натрий (Na) и калий (F). За исключением бериллия, он правильно объединил щелочноземельные элементы: магний (Mg), кальций (Са), стронций (Sr) и барий (Ва). Многочисленные ошибки Ампера связаны с сегодняшней 11-й группой: медь (Сu), серебро (Ag) и золото (Аu) ученый отнес к трем разным видам и даже разным родам. Ампер также не слишком точен в группе кристаллогенов и пниктогенов, поскольку элементы этих групп отнесены к трем и четырем разным видам.
Но самая большая проблема классификации Ампера заключается не в том, насколько верно он объединил элементы в группы. Гораздо важнее то, что ученый не принимал во внимание атомную массу элементов, поэтому современники скептически относились к его работам. На самом деле в сегодняшней периодической таблице элементы объединены не только по их физико-химическим свойствам, но и на основе атомной массы. Предпосылки этой идеи возникли во времена Ампера. Немецкий химик Иоганн Вольфганг Дёберейнер (1780-1849) сделал первый шаг в этом направлении. В 1816 году он заметил, что элементы можно объединять в тройки: центральный элемент будет обладать промежуточной атомной массой по отношению к двум соседним. Эта форма была названа триадами, и некоторые из этих триад таковы: хлор — бром — йод, кальций — стронций — барий, сера — селен — теллур, литий — натрий — калий. Как видно, в некоторых случаях интуиция не подвела Ампера: триада кальций — стронций — барий соответствует девятому виду классификации Ампера (кальциды), а два элемента (хлор и йод) триады хлор — бром — йод присутствуют в четвертом виде (хлориды), в нем нет брома, поскольку он был открыт лишь в 1826 году. Другие ученые, работавшие над классификацией элементов в XIX веке, последовали по пути, открытому Дёберейнером, и в 1869 году русский химик Дмитрий Иванович Менделеев (1834-1907) опубликовал периодическую таблицу элементов, которая приводится в школьных учебниках.
ЗАКОН ОБЪЕМНЫХ ОТНОШЕНИЙ И ГИПОТЕЗА АВОГАДРО — АМПЕРА
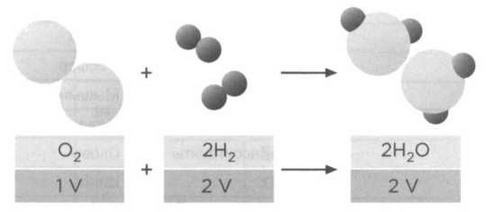
Согласно закону объемных отношений Гей-Люссака один объем (1V) кислорода при соединении с двумя объемами (2V) водорода образует два объема (2 V) воды, то есть вещества, вступающие в реакцию, и вещество, образовавшееся в ее результате, относятся друг к другу как простые числа (1:2:2). Версия Ампера была следующей: частица кислорода — двухатомная молекула в современной терминологии — соединяется с двумя частицами водорода — двумя молекулами в современном смысле, — в результате чего образуется две молекулы воды — две молекулы, состоящие из двух атомов водорода и одного атома кислорода.
Ампер продолжал заниматься химией, хотя так и не заслужил признания современников. Однако в историю науки он вошел не из-за этих исследований. В 1816 году, после отклонения третьего доклада по химии, ученый решил оставить эту область знаний. Неудача, возможно, объясняется событиями, с которыми он столкнулся с 1820 года и которые изменили как исследования Ампера, так и всю его жизнь.
| РОД* | ВИД* | НАЗВАНИЕ ЭЛЕМЕНТА |
| 1. Газолиты | 1. Бориды | Бор |
| Кремний | ||
| 2. Антрациты | Уголь | |
| Водород | ||
| 3. Тиониды | Азот | |
| Сера | ||
| Кислород | ||
| 4. Хлориды | Хлор | |
| Фтор | ||
| Йод | ||
| 5. Арсениды | Теллур | |
| Фосфор | ||
| Мышьяк | ||
| II. Лейколиты | 6. Касситериты | Сурьма |
| Олово | ||
| Цинк | ||
| 7. Аргириды | Висмут | |
| Ртуть | ||
| Серебро | ||
| Свинец | ||
| 8. Тефралиды | Калий | |
| Натрий | ||
| 9. Кальциты | Барий | |
| Стронций | ||
| Кальций | ||
| Магний | ||
| 10. Циркон иды | Иттрий | |
| Бериллий (глюциний) | ||
| Алюминий | ||
| Цирконий |
Жалоба
Напишите нам, и мы в срочном порядке примем меры.





Комментарии