Гейзенберг. Принцип неопределенности - Жозе Наварро Фаус Страница 17
Гейзенберг. Принцип неопределенности - Жозе Наварро Фаус читать онлайн бесплатно
Борн смотрел на ситуацию иначе. Он сразу понял, что формализм Шрёдингера намного лучше, чем матричная механика, подходил для описания частицы, направленной в мишень. Однако Борн также выступил с критикой физических моделей Шрёдингера, так как, по его мнению, ученый попытался вернуться к классической непрерывной теории. Борн предложил «сохранить только формальную сторону этой теории и наделить ее новым физическим смыслом». В июне 1926 года он опубликовал работу о столкновениях квантовых частиц, в которой впервые описал понятие квантовой вероятности. Борн считал, что при изучении столкновений следует отказаться от детерминистского подхода и говорить исключительно о вероятности, с которой частица будет отклоняться в заданном направлении.

Гейзенберг на конференции, 1924 год.

Памятник, установленный на немецком острове Гельголанд.

Макс Борн (слева) и Вольфганг Паули.
Чем больше я размышляю о физической составляющей теории Шрёдингера, тем ужаснее она мне кажется.
Эта вероятность задается волновой функцией Ψ(x), описывающей динамику частицы. Точнее говоря, вероятность того, что частица будет заключена в малом объеме ΔV вокруг точки с координатой х, определяется произведением Ψ(x)|²ΔV Таким образом, с течением времени электрон не занимает все доступное пространство (этот абсурдный вывод следовал из интерпретации Шрёдингера), а всего лишь увеличивается вероятность обнаружить его в любой точке пространства, и эта вероятность постепенно достигает единицы. Появление вероятностей ознаменовало поворотный момент в дискуссиях об интерпретации квантовой механики. Для физиков из Гёттингена и Копенгагена квантовая теория по своей сути была недетерминированной, а следовательно, вероятностная природа была одной из ее важнейших характеристик.
Спин электрона
Описание атомных явлений было завершено с открытием спина электронов. Все началось с того, что в 1924 году Паули занялся изучением модели каркаса атома. Напомним, что в этой модели атом состоит из каркаса, включающего атомное ядро и электроны внутренних уровней, и электронов внешних уровней, связанных с ядром не столь сильно. В объяснении аномального эффекта Зеемана, предложенном Гейзенбергом, момент импульса, слабо связанный с магнитным полем внешних электронов, делился между этими двумя частями атома. Паули не нравилась идея о разделении момента импульса, и он предположил, что электрон описывается четырьмя квантовыми числами: три из них уже были описаны в модели Зоммерфельда, а новое, четвертое, могло принимать одно из двух значений. Паули сформулировал принцип, который сегодня носит его имя: атом не может содержать двух электронов с одинаковыми квантовыми числами. Так стала понятна трактовка периодической системы элементов, предложенная Бором, в которой каждому энергетическому уровню соответствовало определенное число электронов.
На основе результатов Паули голландские физики Сэмюэл Абрахам Гаудсмит и Джордж Юджин Уленбек определили понятие спина электрона. Продолжая аналогию с планетарными системами, они указали, что электрон может вращаться вокруг себя, и это вращение можно измерить. Кроме того, Гаудсмит и Уленбек увидели, что для объяснения двойных линий спектра щелочных металлов требовалось, чтобы соответствующее квантовое число принимало только значения +1/2 и -1/2 и измерялось в тех же единицах, что и редуцированная постоянная Планка % Так воедино были связаны полуцелые числа, модель каркаса атома, принцип Паули и результаты экспериментов. Кроме того, Гейзенберг и Йордан показали, что учет спина электрона в квантовой механике позволял однозначно разрешить эффект Зеемана.
Однако как представить себе электрон, вращающийся вокруг себя? Если электрон подобен точке, то как понимать вращение точки вокруг себя? Если же электрон имеет размер, то скорость точки на экваторе электрона превысит скорость света. Также возникает вопрос, почему электрон не взрывается под действием сил отталкивания между его частями. Аналогии с классической физикой приводили и к другим проблемам подобного рода. Следовало предположить, что спин – это еще одно свойство электрона, подобное его массе, электрическому заряду или магнитному моменту Гейзенберг смог прояснить одно интересное свойство атома гелия. Анализ его спектра выявил существование двух разных последовательностей линий спектра. Ученый посчитал, что, возможно, существуют две разновидности гелия, которые назвал парагелием и ортогелием. Расскажем, как рассуждал Гейзенберг. Сначала он заметил, что электроны неразличимы между собой. Следовательно, волновая функция множества идентичных электронов должна обладать какими-либо свойствами симметрии, отражающими эту особенность электронов.
Опасность классических аналогий
Классические аналогии помогают понять квантовую физику, однако их буквальное применение становится причиной противоречий. В качестве примера приведем сравнение спина электрона с вращательным движением электрона вокруг оси. Рассмотрим сферу с радиусом R и массой М, которая вращается вокруг своей оси с угловой скоростью со (угловая скорость определяется как число оборотов в единицу времени). Скорость точки на экваторе сферы рассчитывается как произведение угловой скорости и радиуса сферы V = ω•R. Момент импульса, связанного с вращательным движением (он представляет собой вектор, сонаправленный с осью вращения), можно записать как произведение момента инерции сферы
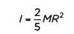
и угловой скорости: L = l•ω. Таким образом, мы можем связать скорость точки на экваторе сферы с моментом импульса вращения:
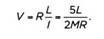
Подставим в указанную формулу параметры электрона и рассмотрим значение скорости. Если мы свяжем момент импульса со спином электрона, то получим L =h/2. В международной системе единиц (метрах, килограммах и секундах) h = 1034 и М = 9•1031 . Чему может быть равно значение R? Оно должно быть меньше размера атома и меньше фемтометра (1015 м) – именно такие размеры имеет ядро атома. Подставив эти числа в предыдущее выражение, получим, что скорость точки на экваторе будет более чем в 500 раз превышать скорость света в вакууме.
Жалоба
Напишите нам, и мы в срочном порядке примем меры.





Комментарии